鐵死亡及其研究進(jìn)展
細(xì)胞程序性死亡是由基因決定的受到分子機(jī)制精密調(diào)控的細(xì)胞主動(dòng),、有序的死亡方式,,與生命體穩(wěn)態(tài)的維持和疾病的發(fā)生密切相關(guān),主要包括焦亡,、壞死和自噬等形式,。鐵死亡是近幾年發(fā)現(xiàn)的一種新的細(xì)胞程序性死亡方式,,作為一種新的細(xì)胞死亡方式已成為科研人員瞄準(zhǔn)的新方向。鐵死亡這一概念最早在2012年由Dr. Dixon [1] 提出,,它是一種鐵依賴性的脂質(zhì)過氧化,、活性氧自由基大量累積所致的細(xì)胞死亡模式,受到多種細(xì)胞代謝途徑的調(diào)控,,其中包括氧化還原穩(wěn)態(tài),、鐵代謝、線粒體活性和氨基酸,、脂質(zhì),、糖的代謝,以及各種與疾病相關(guān)的信號途徑,。研究表明,,鐵死亡與器官損傷、神經(jīng)退行性疾病,、心血管疾病,、炎癥性疾病、癌癥相關(guān),。特別是具有多重藥物抗藥性的癌細(xì)胞,,尤其是處于間充質(zhì)狀態(tài)且易于轉(zhuǎn)移的腫瘤細(xì)胞,非常容易發(fā)生鐵死亡,。因此,,通過誘導(dǎo)和抑制鐵死亡對其進(jìn)行藥理調(diào)節(jié),在治療耐藥性癌癥,、缺血性器官損傷和其他與脂質(zhì)過氧化密切相關(guān)的退行性疾病上具有巨大的潛力,。

圖1 細(xì)胞死亡的分類
鐵死亡的生化特點(diǎn): 鐵死亡又名鐵壞死,是一種與活性氧(reactive oxygen species, ROS)聚集有關(guān)的細(xì)胞死亡形式,,其本質(zhì)為鐵蓄積和脂質(zhì)過氧化,。細(xì)胞抗氧化體系代謝異常時(shí),Fe2+蓄積能夠介導(dǎo)芬頓(Fenton)反應(yīng)產(chǎn)生過量ROS(尤其是羥自由基),,ROS與細(xì)胞膜上的多不飽和脂肪酸(polyunsaturated fatty acid, PUFA)發(fā)生過氧化反應(yīng),,導(dǎo)致脂質(zhì)雙分子層穩(wěn)定性遭到破壞,細(xì)胞膜解體,,進(jìn)而促進(jìn)細(xì)胞鐵死亡[1] ,。

圖3 鐵死亡的主要途徑
2.鐵死亡主要途徑
鐵死亡可通過外源性或內(nèi)源性途徑誘發(fā)。
2.1外源性 (轉(zhuǎn)運(yùn)蛋白依賴) 途徑
2.1.1氨基酸代謝—抑制胱氨酸/谷氨酸轉(zhuǎn)運(yùn)蛋白 [5]
System xc-是細(xì)胞內(nèi)重要的抗氧化體系,該系統(tǒng)由2個(gè)亞基組成,SLC7A11和SLC3A2。SLC7A11負(fù)責(zé)主要的轉(zhuǎn)運(yùn)活性,,對胱氨酸和谷氨酸有高度特異性,,而 SLC3A2則作為伴侶蛋白,。System xc-以1:1的比例用胞內(nèi)谷氨酸來換取胞外的胱氨酸(Cys2),胱氨酸在谷氨酸半胱氨酸連接酶(GCL)和谷胱甘肽合成酶(GSS)的催化作用下合成谷胱甘肽(GSH)(GSH是膜脂修復(fù)酶-谷胱甘肽過氧化物酶(GPX4)的還原性輔因子),。抑制 System xc- 的活性會抑制胱氨酸的吸收,,影響GSH的合成,繼而導(dǎo)致膜脂修復(fù)酶GPX4活性降低,,細(xì)胞抗氧化能力降低,,從而促進(jìn)鐵死亡。
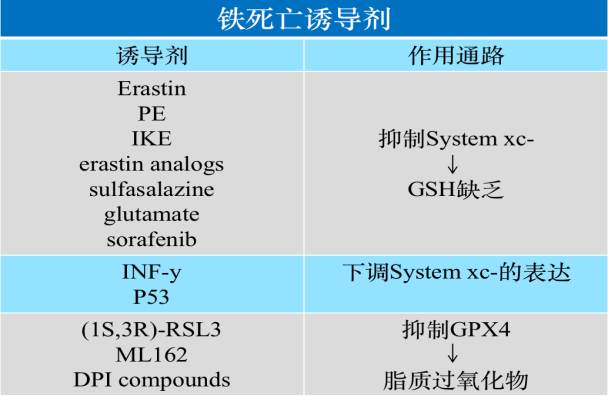
表2 目前已知的部分鐵死亡誘導(dǎo)劑及作用通路
2.1.2鐵代謝—轉(zhuǎn)運(yùn)蛋白與鐵“超載” [6-7]
鐵具有Fe2+和Fe3+兩種氧化態(tài),。食物中Fe3+在腸道被還原為Fe2+后被小腸上皮細(xì)胞吸收,。Fe2+在膜鐵轉(zhuǎn)運(yùn)蛋白的作用下被運(yùn)輸至細(xì)胞外并被氧化為Fe3+,與轉(zhuǎn)鐵蛋白(transferrin, TF)(血清轉(zhuǎn)鐵蛋白或乳鐵蛋白)結(jié)合形成TF-Fe3+復(fù)合物,,經(jīng)血液循環(huán)運(yùn)輸至各組織器官,。Fe3+與細(xì)胞膜上的轉(zhuǎn)鐵蛋白受體(TFRC)結(jié)合進(jìn)入細(xì)胞內(nèi)后被金屬還原酶STEAP3還原為Fe2+,,然后通過二價(jià)金屬轉(zhuǎn)運(yùn)蛋白1將Fe2+釋放到胞質(zhì)的動(dòng)態(tài)鐵池中,。正常生理狀態(tài)下,動(dòng)態(tài)鐵池可以維持鐵平衡,。
病理情況下,,Fe 2+在細(xì)胞內(nèi)集聚,發(fā)生哈伯-韋斯反應(yīng)(Haber-Weiss)與Fenton反應(yīng),,產(chǎn)生大量ROS,與細(xì)胞膜上的多不飽和脂肪酸PUFA發(fā)生一系列過氧化反應(yīng),,生成脂質(zhì)過氧化物,,破壞細(xì)胞膜結(jié)構(gòu)并引起細(xì)胞鐵死亡。同時(shí)Fe2+作為多種代謝鐵的積累是鐵死亡過程中啟動(dòng)膜氧化的關(guān)鍵信號之一,;TF通過TFRG介導(dǎo)鐵攝取,,FTH1/FTL (鐵蛋白組件)通過自噬降解可以增加鐵的水平并促進(jìn)鐵死亡。
SLC40A1介導(dǎo)的鐵外流和外泌體介導(dǎo)的鐵蛋白輸出會抑制鐵死亡,。
2.2內(nèi)源性 (酶調(diào)控) 途徑
2.2.1脂質(zhì)代謝—多不飽和脂肪酸PUFAs過氧化[8-9]
鐵死亡的中心環(huán)節(jié)是鐵依賴的脂質(zhì)氧化代謝失調(diào),,多不飽和脂肪酸(PUFAs)是鐵死亡中脂質(zhì)過氧化物積累的關(guān)鍵物質(zhì)。 正常情況下,,PUFAs 是脂質(zhì)代謝的重要底物,,含有雙烯丙基氫原子,尤其是花生四烯酸(arachidonoyl, AA)和腎上腺素酸(adrenoyl, AdA),,易與ROS發(fā)生反應(yīng),,引起脂質(zhì)過氧化。當(dāng)長鏈脂酰輔酶A合成酶4(ACSL4)催化游離的AA或AdA與輔酶A(coenzyme A, CoA)結(jié)合形成衍生物AA-CoA或AdA-CoA,然后被溶血卵磷脂?;D(zhuǎn)移酶3(LPCAT3)酯化為膜磷脂酰乙醇胺(PEs),,并經(jīng)過脂氧合酶(ALOXs)或細(xì)胞色素P450氧化還原酶(POR)氧化后,就形成了有害的脂質(zhì)過氧化產(chǎn)物,,誘導(dǎo)細(xì)胞鐵死亡,。
乙酰輔酶A羧化酶(ACAC)介導(dǎo)的脂肪酸合成,脂質(zhì)吞噬(Lipophagy)介導(dǎo)的脂肪酸釋放,,可誘導(dǎo)細(xì)胞內(nèi)游離脂肪酸的積累,,促進(jìn)鐵死亡。
2.2.2其他代謝途徑
CoQ10能被鐵死亡抑制蛋白1(ferroptosis suppressor protein 1, FSP1)還原來阻止脂質(zhì)氧化進(jìn)而抑制鐵死亡,。
NADPH能參與GSH-GPX4抗氧化系統(tǒng)的循環(huán),,其大量消耗將限制GSH-GPX4的抗氧化功能,誘導(dǎo)鐵死亡,。
硒是維持GPX4活性的一種必需的微量營養(yǎng)素,,通過協(xié)同激活轉(zhuǎn)錄因子TFAP2c和Sp1調(diào)節(jié)GPX4的豐度和活性,在一定程度上抑制鐵死亡以保護(hù)神經(jīng)元,。
NFE2L2可通過反式激活的方式調(diào)控包括鐵代謝,、GSH代謝以及抗ROS過程中的基因的表達(dá)進(jìn)而限制鐵死亡過程中的氧化損傷。
Vitamin E通過抑制ALOXs活性,、減少脂質(zhì)過氧化物的產(chǎn)生,,從而抑制鐵死亡。
p53可以通過下調(diào)Xc-系統(tǒng)組分SLC7A11的表達(dá),,抑制胱氨酸的攝取,,從而誘導(dǎo)細(xì)胞鐵死亡;同時(shí)p53可以抑制二肽基肽酶-4(dipeptidyl peptidase-4, DPP4)的活性,,阻斷Erastin誘導(dǎo)的鐵死亡,。
NRF2是維持細(xì)胞內(nèi)氧化還原穩(wěn)態(tài)的重要調(diào)控因子,通過p62-Keap1-NRF2途徑上調(diào)參與鐵和ROS代謝的多種基因(NQO1,、HO1和FTH1)的表達(dá),,抑制細(xì)胞鐵死亡,。
3鐵死亡在疾病治療中的應(yīng)用
鐵死亡與癌癥,、衰老、神經(jīng)退行性疾病,、心肌病,、中風(fēng)、腦出血?jiǎng)?chuàng)傷性腦損傷,、缺血
再灌注損傷和腎臟變性相關(guān)的病理細(xì)胞死亡有關(guān),。
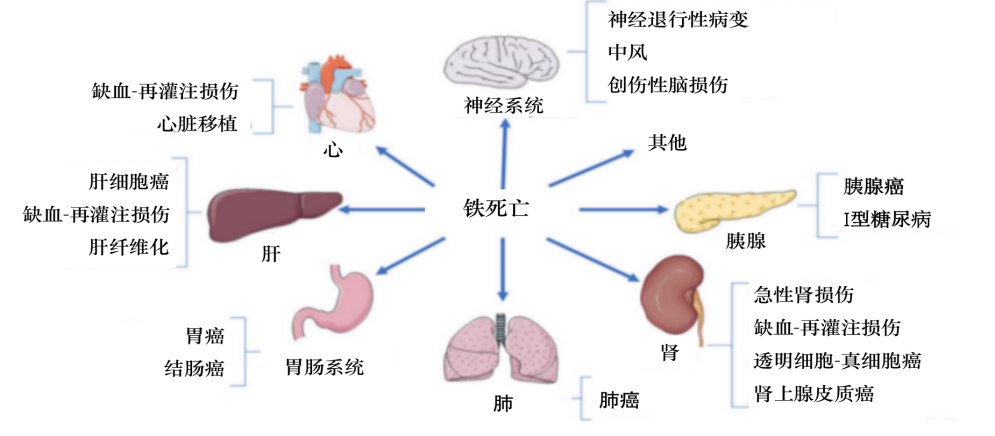
圖5 鐵死亡相關(guān)疾病
3.1 癌癥
研究表明許多癌癥相關(guān)基因和信號通路都能調(diào)控鐵死亡,,誘導(dǎo)癌細(xì)胞鐵死亡對治療癌癥意義重大。對凋亡和常規(guī)癌癥療法抵抗的間充質(zhì)干細(xì)胞和去分化的癌細(xì)胞,,以及被稱為“持續(xù)細(xì)胞”的癌細(xì)胞都對鐵死亡誘導(dǎo)高度敏感,。與正常細(xì)胞相比,癌細(xì)胞代謝比較旺盛,,線粒體出現(xiàn)功能障礙,,ROS積累較多,增加了癌細(xì)胞對鐵死亡的敏感性,。
卵巢癌:實(shí)驗(yàn)證實(shí)在卵巢癌中可通過TAZ-ANGPTL4-NOX2信號軸激活鐵死亡抑制卵巢癌細(xì)胞的增殖,。
結(jié)、直腸癌:細(xì)胞紅蛋白(cytoglob, CYGB)是ROS的細(xì)胞調(diào)節(jié)劑,,也是一種腫瘤抑制劑,,能夠促進(jìn)細(xì)胞膜上的脂質(zhì)過氧化進(jìn)而抑制結(jié)直腸癌細(xì)胞的生長,過表達(dá)CYGB的結(jié)直腸癌細(xì)胞對RSL3和Erastin誘導(dǎo)的鐵死亡更敏感,,敲除Yes相關(guān)蛋白1基因YAP1可通過減輕ROS的產(chǎn)生降低結(jié),、直腸癌細(xì)胞對鐵死亡的敏感性。
另外,,癌癥的治療可以通過靶向氨基酸,、脂質(zhì)、鐵代謝相關(guān)信號通路進(jìn)行,。
3.2 衰老和神經(jīng)退行性疾病
在衰老和退行性疾病如帕金森病(Parkinson's disease, PD),、亨廷頓病和阿爾茨海默病(Alzheimer's disease, AD)的患者中檢測到鐵水平升高,其原因可能是隨著年齡的增長,,鐵的代謝速率不斷降低,導(dǎo)致機(jī)體鐵過量和過氧化損傷,,最終引起細(xì)胞死亡,。
多種證據(jù)表明,GSH-GPX4抗氧化通路在AD和PD患者中均出現(xiàn)明顯異常,,使用抗氧化藥物可以緩解AD與PD病理癥狀,。
研究顯示,使用鐵死亡抑制劑能夠保護(hù)帕金森病模型小鼠免受過氧化損傷,。
大鼠海馬切片培養(yǎng)的離體實(shí)驗(yàn)表明,,鐵死亡抑制劑ferrostatin-1可阻斷谷氨酸誘導(dǎo)的神經(jīng)元興奮毒性細(xì)胞死亡。
遺傳學(xué)研究一致證實(shí),,小鼠條件性缺失Gpx4會引起類似神經(jīng)退行性病變的癥狀,。
3.3缺血再灌注損傷
缺血再灌注損傷是一種無菌性炎癥。器官或組織缺血一段時(shí)間后重新獲得血液供應(yīng),,但缺血性損傷不但沒有減輕反而進(jìn)一步加重,,甚至出現(xiàn)更嚴(yán)重的細(xì)胞代謝功能障礙或結(jié)構(gòu)破壞,。在腦缺血-再灌注損傷中鐵蓄積和脂質(zhì)過氧化等現(xiàn)象與鐵死亡一致,且這一現(xiàn)象可以被鐵螯合劑或抗氧化劑抑制,。
在小鼠心臟缺血-再灌注損傷模型中,,在再灌注開始時(shí)給予抑制鐵死亡的小分子化合物Liproxstatin-1能夠增加線粒體內(nèi)GPX4的含量,降低線粒體內(nèi)ROS的產(chǎn)生,,降低缺血性梗死面積并改善線粒體結(jié)構(gòu)和功能,。
在糖尿病大鼠心臟缺血-再灌注模型中發(fā)現(xiàn),, ROS與內(nèi)質(zhì)網(wǎng)應(yīng)激相互聯(lián)系是引發(fā)鐵死亡的重要因素,其能夠進(jìn)一步造成心臟缺血-再灌注損傷,。
在缺血-再灌注損傷小鼠模型,、Gpx4全身敲除小鼠和葉酸誘導(dǎo)急性腎損傷小鼠模型中,鐵死亡抑制劑已被證明可以減輕腎小管細(xì)胞死亡和急性腎功能衰竭,。
肝細(xì)胞特異性Gpx4敲除小鼠出生不久即會死亡,,但高水平的維生素E飲食可以彌補(bǔ)肝臟中GPX4的缺乏,使小鼠存活,。
此外Liproxstatin-1(一種強(qiáng)效鐵死亡抑制劑)能保護(hù)肝實(shí)質(zhì)組織免受缺血-再灌注損傷,。
3.4心腦血管疾病
發(fā)生腦卒中時(shí),胞內(nèi)脂質(zhì)過氧化物及 Fe2+水平升高,,而使用鐵死亡抑制劑上調(diào) GSH,、GPX4或 System xc-水平均可減輕腦部損傷,這表明鐵死亡介導(dǎo)了腦卒中,。近年研究進(jìn)一步發(fā)現(xiàn),,機(jī)體鐵過載會降低動(dòng)脈斑塊的穩(wěn)定性,使用鐵螯合劑可縮小動(dòng)脈斑塊面積,,減輕動(dòng)脈粥樣硬化的發(fā)展,。心肌細(xì)胞凋亡是心力衰竭的重要病理變化,但研究表明心力衰竭過程中除細(xì)胞凋亡外還有鐵死亡的參與,,且兩者獨(dú)立并存,。
4細(xì)胞鐵死亡的檢測
4.1形態(tài)學(xué)檢測
超微形態(tài)學(xué)特征顯示細(xì)胞膜斷裂和出泡,線粒體變小,、膜密度增高,、線粒體脊減少或消失、線粒體外膜斷裂,,細(xì)胞核大小正常,、但缺乏染色質(zhì)凝聚,。電鏡下表現(xiàn)為細(xì)胞內(nèi)線粒體變小及雙層膜密度增高。
4.2生物學(xué)特征
*鐵死亡的金指標(biāo):脂質(zhì)過氧化物(Lipid peroxidation)
鐵和活性氧(ROS)聚集,,激活絲裂原活化蛋白激酶(mitogen-activatedprotein kinase,,MAPK)系統(tǒng),通過降低胱氨酸的攝取,、耗竭谷胱甘肽,,抑制ystem Xc-和增加還原型酰腺嘌呤二核苷酸磷酸氧化酶,釋放花生四烯酸等介質(zhì),。細(xì)胞內(nèi)活性氧和脂質(zhì)活性氧通過流式細(xì)胞術(shù)使用DCFH-DA,、C11-BODIPY 和Liperfluo檢測。
在細(xì)胞培養(yǎng)基中添加藥物后,,脂質(zhì)過氧化物染色(Liperfluo)檢測Lipid peroxidation,,如為陽性結(jié)果,證明鐵死亡發(fā)生,;若在上述添加藥物的細(xì)胞培養(yǎng)基中添加鐵死亡抑制劑后,,檢測Lipid peroxidation為陰性結(jié)果,證明藥物誘導(dǎo)的一定是鐵死亡,,而非其他死亡方式,。
C11-BODIPY對自由基非常敏感,但不和脂質(zhì)過氧化物反應(yīng),,Liperfluo是目前唯一可以特異性檢測脂質(zhì)過氧化物的化合物,。
4.3鐵水平檢測
可以使用PGSK探針,流式細(xì)胞術(shù)或共聚焦顯微鏡檢測細(xì)胞內(nèi)鐵含量的細(xì)胞膜透性染料,;或者使用Iron Assay Kit(試劑盒)檢測細(xì)胞,、組織中的鐵水平。
實(shí)驗(yàn)原理:通常利用鐵離子氧化狀態(tài)的過渡性改變來進(jìn)行各種化學(xué)反應(yīng),。通過加入酸性緩沖液來釋放鐵離子,,樣品中的Fe2+可直接測定,或通過還原反應(yīng)來測定鐵元素(Fe2+和Fe3+)總含量,。反應(yīng)釋放出的鐵元素與生色團(tuán)反應(yīng),生成與樣品中的鐵成正比的比色(593 nm)產(chǎn)物,。
4.4細(xì)胞活性檢測
可以使用MTT/CCK8法檢測細(xì)胞活性,。
4.5線粒體膜電位檢測
可以使用TMRE熒光染料檢測,TMRE能夠特異性標(biāo)記有活性的線粒體,,是一種細(xì)胞膜可穿透性的,,正電荷的,橘紅色熒光染料,。當(dāng)線粒體膜電位降低時(shí),,熒光減弱,。
實(shí)驗(yàn)原理:TMRE (tetramethylrhodamine, ethyl ester),中文名稱叫做四甲基羅丹明乙酯,,CAS號為115532-52-0,,分子式為C26H27CIN2O7,分子量為515,。TMRE是一種可滲透細(xì)胞膜的橘紅色陽離子熒光探針,,可在完整的線粒體中聚集,而去極化或非活躍性線粒體膜電位降低,,導(dǎo)致TMRE積聚減少,。檢測時(shí)TMRE的最大激發(fā)波長為550nm,最大發(fā)射波長為575nm,。正常狀態(tài)下的線粒體內(nèi)部存在大量的負(fù)電荷,,作為陽離子探針的TMRE進(jìn)入細(xì)胞內(nèi)后可聚集在線粒體基質(zhì)中,可發(fā)出明亮的橘紅色熒光,;當(dāng)細(xì)胞發(fā)生凋亡時(shí),,線粒體膜電位丟失,線粒體通透性轉(zhuǎn)換孔(MPTP)持續(xù)開放,,TMRE被釋放到細(xì)胞質(zhì)中,,線粒體內(nèi)橘紅色熒光強(qiáng)度明顯下降??捎脽晒怙@微鏡,、流式細(xì)胞儀、熒光酶標(biāo)儀等儀器檢測細(xì)胞,,通過熒光信號的強(qiáng)弱來確定線粒體膜電位的變化和凋亡或壞死的發(fā)生,。
4.6 qRT-PCR/Western blot檢測
檢測細(xì)胞內(nèi)與鐵死亡相關(guān)的因子的變化,例如COX-2,,ACSL4,,PTGS2,NOX1,,GPX4和FTH1等,,其中COX-2,ACSL4,,PTGS2和NOX1在鐵死亡細(xì)胞中表達(dá)上調(diào),;GPX4和FTH1在鐵死亡細(xì)胞中表達(dá)下調(diào)。
參考文獻(xiàn):
[1]Dixon SJ, Lemberg KM, Lamprecht MR, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell, 2012, 149(5): 1060-1072.
[2]陳璐瑤,饒小珍.鐵死亡的發(fā)生機(jī)制及相關(guān)疾病研究進(jìn)展[J].生物學(xué)教學(xué),2022,47(02):2-5.
[3]Jiang X, Stockwell BR, Conrad M.Ferroptosis: mechanisms, biology and role in disease.Nat Rev Mol Cell Biol, 2021,22(4):266-282.
[4]Daolin Tang, Xin Chen, Rui Kang, Guido Kroemer. Broadening horizons: the role of ferroptosis in cancer. Nat Rev Clin Oncol. 2021 Jan 29.
[5]Piani D, Fontana A. Involvement of the cystine transport system xc- in the Macrophage
-induced glutamate-dependent cytotoxicity to neurons. J Immunol, 1994, 152(7): 3578-3585.
[6] Outten FW, Theil EC. Iron-based redox switches in biology. Antioxid Redox Signal, 2009, 11(5): 1029-1046
[7] Gao M, Monian P, Quadri N, et al. Glutaminolysis and transferrin regulate ferroptosis. Mol Cel, 2015, 59(2): 298-308
[8]Yang WS, Kim KJ, Gaschler MM, et al. Peroxidation of polyunsaturated fatty acids by lipoxygenases drives ferroptosis. Proc Natl Acad Sci USA, 2016, 113(34): E4966-E4975
[9]Doll S, Proneth B, Tyurina YY, et al. ACSL4 dictates ferroptosis sensitivity by shaping cellular lipid composition. Nat Chem Biol, 2017, 13(1): 91-98


